Messung der Oberflächenspannung
Oberflächenspannung
Die Oberflächenspannung σ (Sigma) ist eine Eigenschaft einer Flüssigkeit (z.B. Wasser) an der Grenzfläche zu einem Gas (z.B. Luft). Sie ist in vielen industriellen Prozessen von Bedeutung, z.B. bei der Benetzung von Oberflächen.
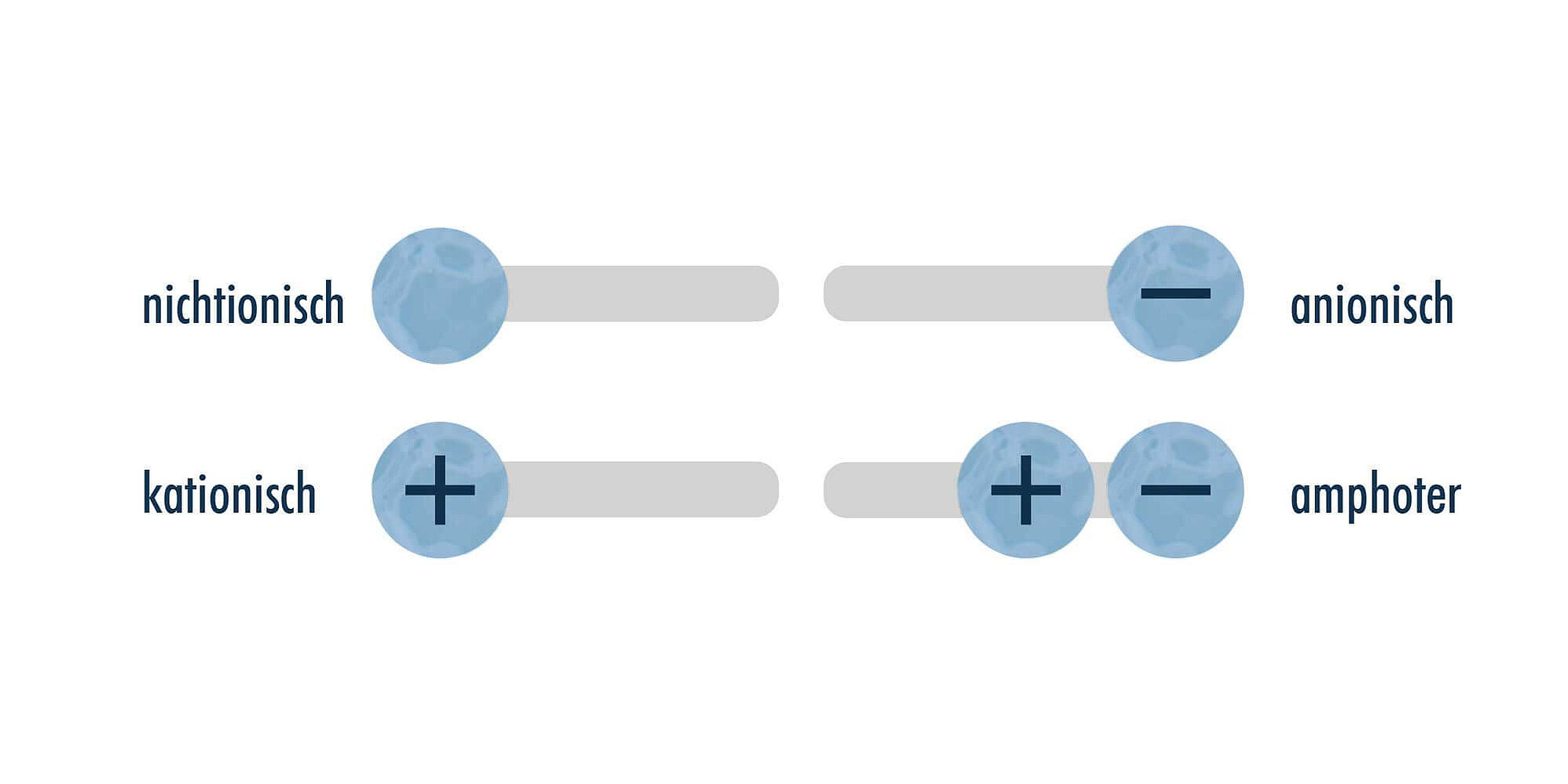
In einer Flüssigkeit stehen die Moleküle miteinander in Wechselwirkung. Kohäsionskräfte bewirken, dass sich die Moleküle anziehen. An der Oberfläche der Flüssigkeit erzeugen diese Kohäsionskräfte eine Spannung, ähnlich einer Haut, die immer bestrebt ist, die Oberfläche so klein wie möglich zu halten. Besonders deutlich wird dieser Effekt bei Wassertropfen, deren runde Form durch eben diese nach innen gerichteten Kräfte entsteht.[1].
Beschrieben wird die Oberflächenspannung als Arbeit, die aufgebracht werden muss, um die Oberfläche um ein bestimmtes Maß zu vergrößern:
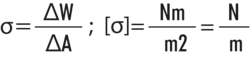
Die Angabe der Oberflächenspannung erfolgt in mN/m oder dyne/cm. Die Oberflächenspannung von Wasser bei 20 °C beträgt 72,75 mN/m (vgl. Ethanol 22,55 mN/m). Für viele wässrige Anwendungen muss die Oberflächenspannung herabgesetzt werden. Hier kommen Tenside zum Einsatz.
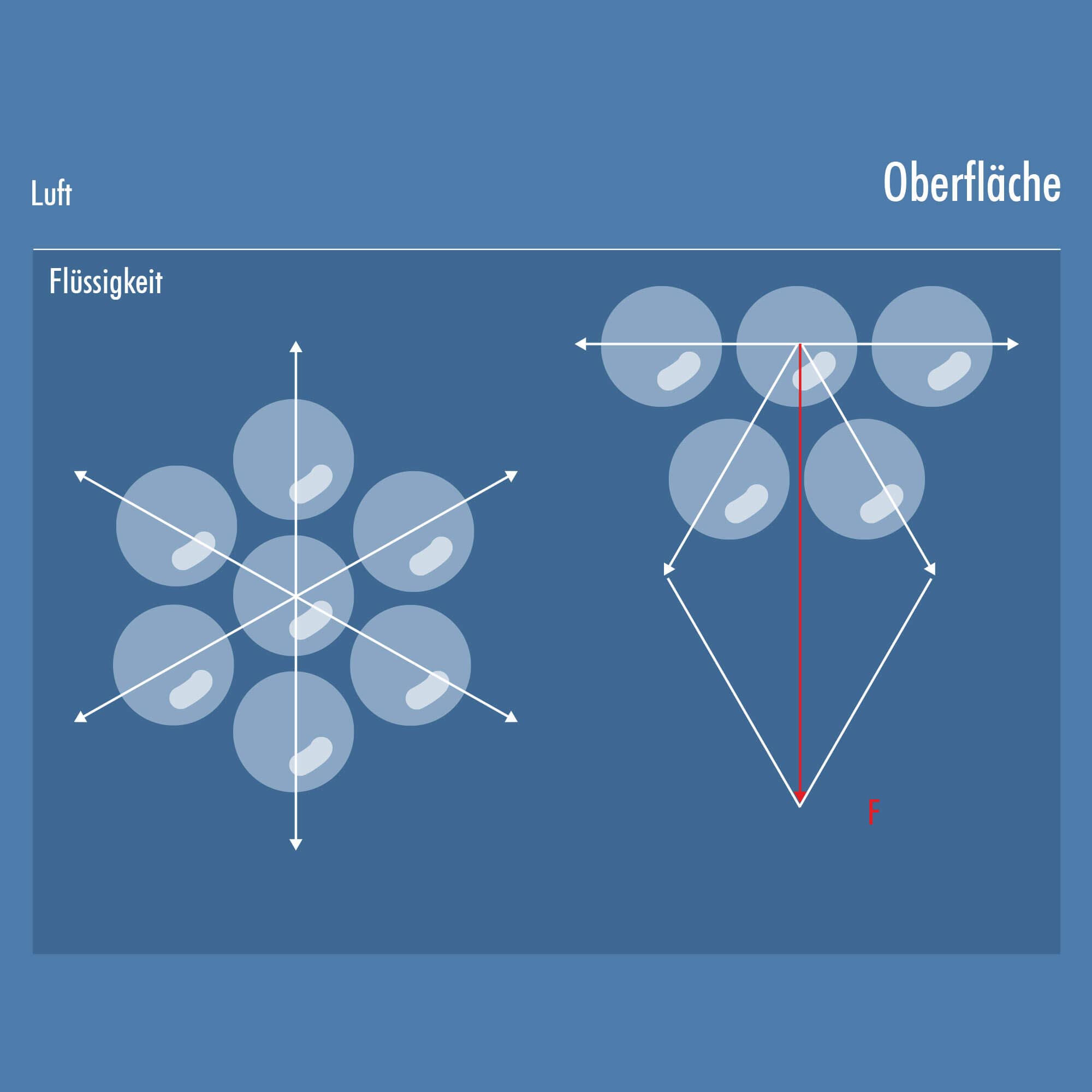
Tenside
Als Tenside wird eine Gruppe chemischer Verbindungen bezeichnet, die aus zwei gegensätzlichen Molekülteilen bestehen: einem unpolaren, hydrophoben Kohlenwasserstoffteil (im Bild: graue Stäbchen) und einer polaren, hydrophilen Kopfgruppe (im Bild: blau Kugeln). Je nach Art der Kopfgruppe unterscheidet man nichtionische, anionische, kationische und amphotere Tenside. Für Anwendungen in der wässrigen Teilereinigung werden hauptsächlich nichtionische und anionische Tenside eingesetzt. Kationische Tenside wirken in Weichspülern oder als Hydrophobierungsmittel auf Oberflächen. Amphotere Tenside wiederum werden in vielen Haut- und Haarwaschmitteln eingesetzt.
Die beiden Molekülteile verhalten sich Wasser gegenüber sehr gegensätzlich: Der hydrophobe Teil wendet sich vom Wasser ab, während der hydrophile Teil dem Wasser zugeneigt ist. Aufgrund dieser so gegensätzlichen Bausteine bewegen sie sich in wässriger Umgebung zu Oberflächen hin[2].
Solche Oberflächen sind z.B. die Grenzflächen Wasser-Luft, Wasser-Festkörper oder auch Wasser-Öl. An der Oberfläche nehmen die Tenside Plätze zwischen den Wassermolekülen ein, stören dort die Kohäsion und senken auf diese Weise die Oberflächenspannung. Dieses Verhalten bezeichnet man als oberflächenaktiv. Die Bewegung der Tenside hin zu einer Oberfläche ist zeitabhängig und wird u.a. beeinflusst von Tensidart und -konzentration, Temperatur und der Flüssigkeit, die sie umgibt (sog. Matrixeffekte).
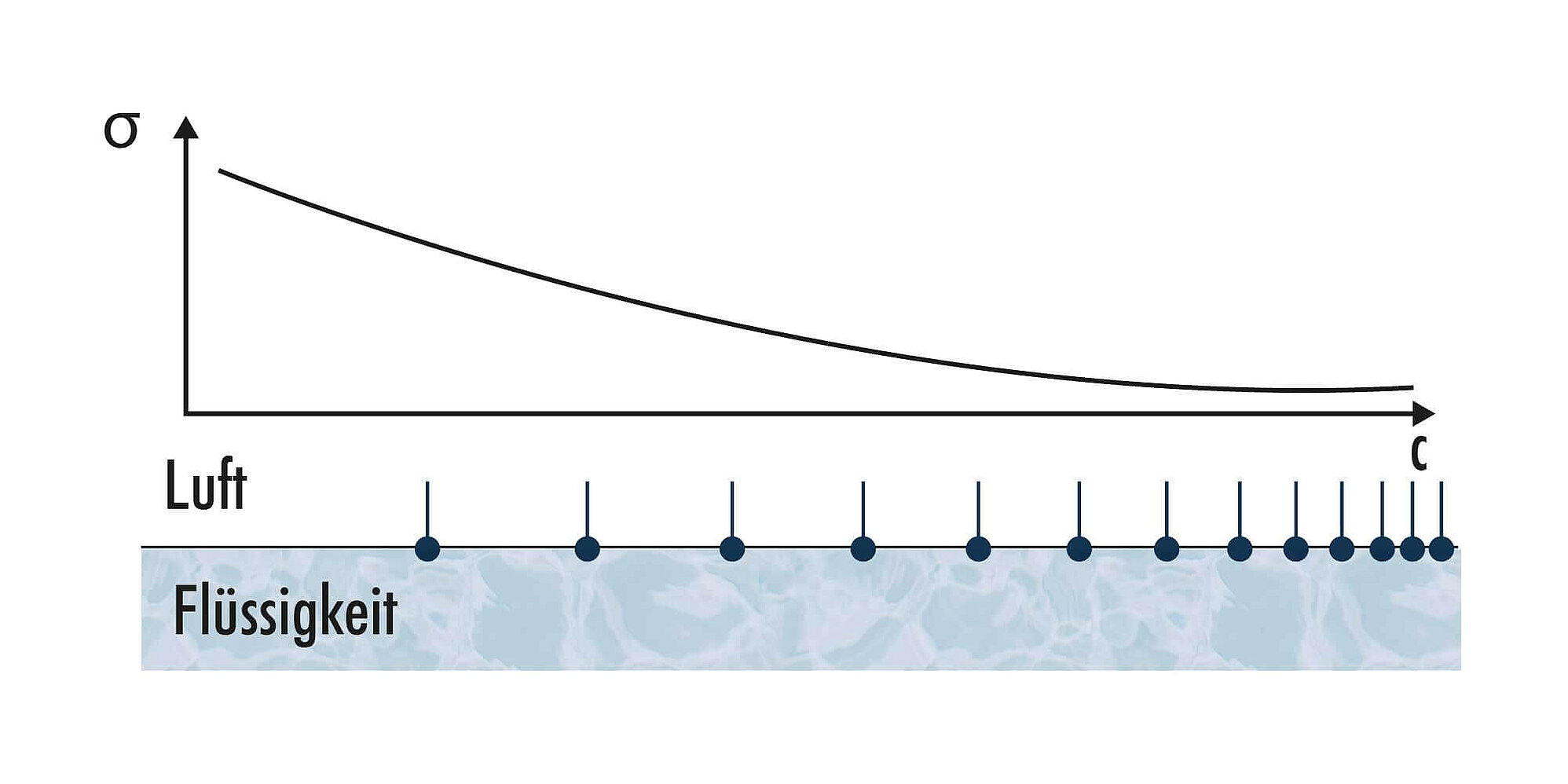
Das oberflächenaktive Verhalten der Tenside, auch Netzmittel genannt, wird in technischen Anwendungen gezielt für vielfältige Effekte ausgenutzt, zum Beispiel:
- Benetzen von Oberflächen
- Entfernen von Ölen und Fetten von Oberflächen
- Emulgieren von Öl in Wasser und Dispergieren von Pigmenten u.ä.
- Schaumbildung oder -vermeidung
- Tropfenbildung und Einstellen der Tropfengröße
Da Tenside die Oberflächenspannung herabsetzen, kann umgekehrt aus der gemessenen Oberflächenspannung der Gehalt an freien Tensiden bestimmt werden, der für technische Anwendungen zur Verfügung steht.
Blasen-Differenzdruck-Verfahren
Verfahren zur Messung der Oberflächenspannung müssen die Oberfläche etwa durch Ziehen oder Drücken gezielt vergrößern. Beim Blasen-Differenzdruck-Verfahren geschieht dies durch das Erzeugen einer Luftblase an einer Kapillarspitze. Alle SITA-Tensiometer arbeiten nach diesem Verfahren, wodurch die Messwerte miteinander vergleichbar sind.
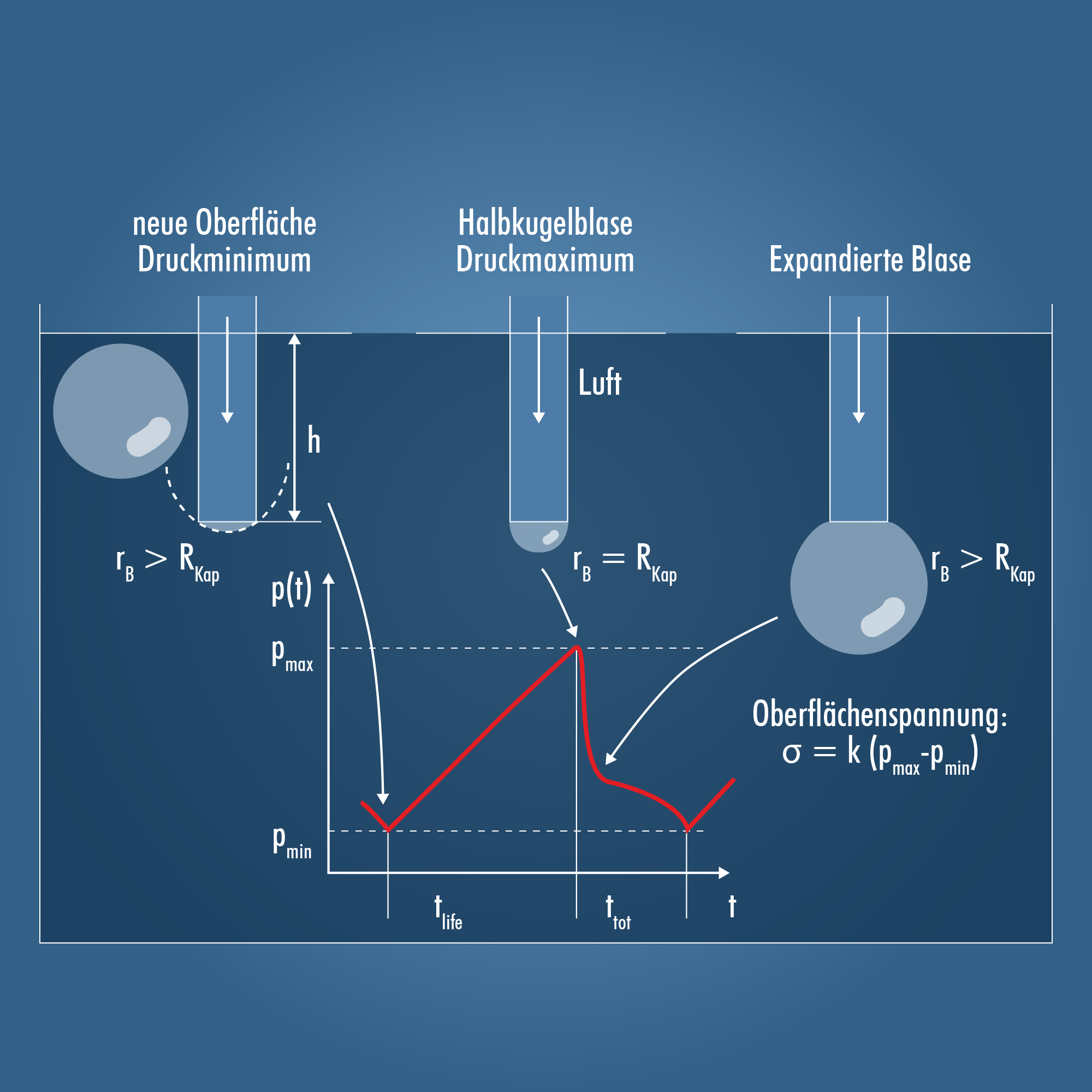
Durch eine Kapillare wird Luft in die Flüssigkeit eingeleitet, wodurch an der Kapillarspitze eine Luftblase entsteht. Kontinuierlich wird der Druck im (Luft-)Volumenstrom gemessen. Die Luftblase durchläuft drei Zustände, wie im Bild rechts dargestellt:
- Kurz nach Abriss einer Luftblase von der Kapillare wird durch den Kapillareffekt die Grenzfläche in die Kapillare hineingezogen. Ein Druckminimum entsteht (oben links).
- Durch das Einleiten von Luft bläst sich die Blase auf bis an den Punkt, an dem der Blasenradius dem Kapillarradius gleicht und ein Druckmaximum erreicht wird (oben mittig). Man bezeichnet das als Halbkugelblase.
- Wird noch mehr Luft eingeleitet, expandiert die Blase schlagartig (oben rechts). Das Volumen vergrößert sich, der Druck nimmt ab. Kurz danach reißt die Blase von der Kapillare ab und der Vorgang beginnt erneut.
Die Differenz zwischen Minimaldruck pmin und Maximaldruck pmax ist nach der Young-Laplace-Gleichung proportional der Oberflächenspannung σ:
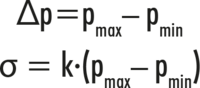
Der Kalibrierfaktor k beinhaltet die bei der Kalibrierung ermittelten fluiddynamischen Eigenschaften der verwendeten Kapillare und Systemparameter des Tensiometers. Im Rahmen der Mehrpunkt-Kalibrierung wird dieser systemische Faktor k in Abhängigkeit verschiedener Blasenlebensdauern tlife ermittelt.
Dynamische und statische Oberflächenspannung
SITA-Tensiometer nutzen zur Messung der Oberflächenspannung das Blasen-Differenzdruck-Verfahren. Bei diesem Verfahren steht die gemessene dynamische Oberflächenspannung stets in Abhängigkeit des Parameters Blasenlebensdauer tlife, gleichbedeutend der Benetzungszeit bzw. dem Oberflächenalter. Das Blasen-Differenzdruck-Verfahren zählt zu den dynamischen Messmethoden.
Weitere dynamische Messmethoden sind die Tropfenvolumenmethode per Stalagmometer oder die Grenzflächenrheologie an einem hängenden Tropfen. Methoden zur Messung der statischen Oberflächenspannung sind z.B. die Ringmethode nach Du Noüy oder die Plattenmethode nach Wilhelmy.
Bei dynamischen Methoden wie der Blasendrucktensiometrie wird ein quasistatischer Wert der Oberflächenspannung im Vergleich zu statischen Methoden erst bei hohen Tensidkonzentrationen c bzw. nach langen Blasenlebensdauern tlife erreicht. Dadurch ist die zur Konzentrationsbestimmung nötige eindeutige Korrelation zwischen Oberflächenspannung und Konzentration auch oberhalb der kritischen Mizellbildungskonzentration cmc[2] gegeben. Bei der Oberflächenspannungsmessung tensidfreier, nicht-oberflächenaktiver Flüssigkeiten (z.B. Lösungsmittel) unterscheiden sich dynamische und statische Methoden nicht.
Wird in Messvorschriften oder der Literatur eine Oberflächenspannung genannt ohne Angabe eines Oberflächenalters oder des Parameters Blasenlebensdauer tlife, ist von einer statischen Oberflächenspannung auszugehen.
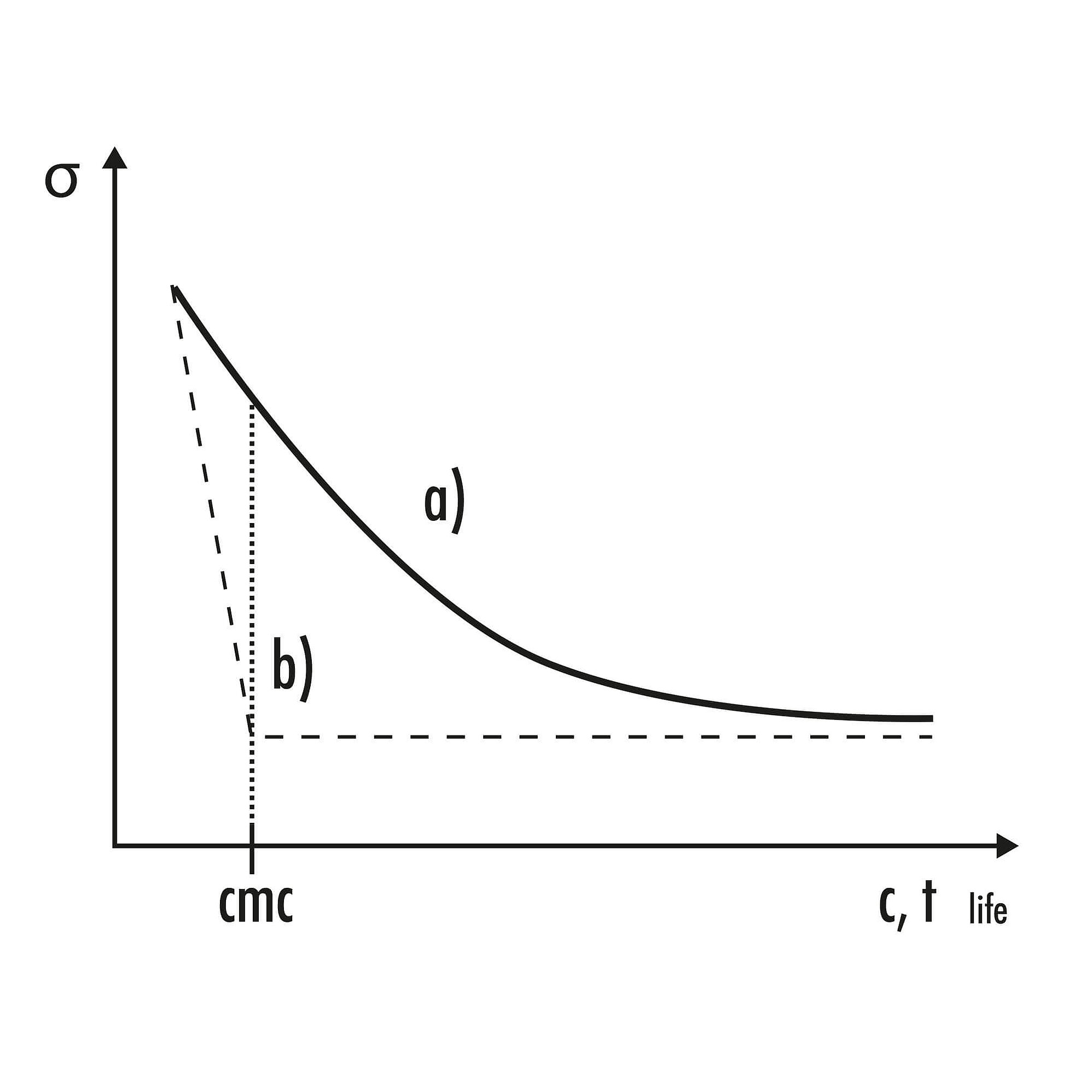
1 In Wasser wirken vorrangig Wasserstoffbrückenbindungen, während in unpolaren Flüssigkeiten Van-der-Waals-Kräfte die Kohäsion bewirken. Diese zwischenmolekularen Kräfte halten die Moleküle zusammen. Die Eigenschaften der Oberflächenschicht der Flüssigkeit unterscheidet sich jedoch von der Volumenphase. Die Anziehungskraft aus der Volumenphase wirkt immer noch auf die Moleküle der Flüssigkeit in der Nähe der Grenzfläche. Somit entsteht eine resultierende Kraft, die in das Innere der Flüssigkeit gerichtet ist.
2 Genauer gesagt stört die Kohlenstoffkette des hydrophoben Teils die Ausbildung der Wasserstoffbrückenbindungen, wodurch dieser Teil des Tensids vom Wasser weggeschoben wird. Da in der Chemie alles nach einem energetisch günstigen Zustand strebt, wird so lange geschoben, bis die Kohlenstoffkette komplett vom Wasser weg zeigt. Das tritt ein, wenn sie aus der Grenzfläche heraus- oder zu einem (ebenso hydrophoben) Öltropfen hinragt. Wenn keine Grenzfläche in der Nähe ist, bilden sich Mizellen. Das sind kleine Tensidtröpfchen, bei denen die hydrophoben Enden ins Innere zeigen und die hydrophilen Kopfgruppen nach außen. Die spezifische Konzentration, bei der dieser Prozess startet, nennt man kritische Mizellbildungskonzentration cmc.